来自我校生命科学学院和化学化工学院的一项最新研究或为未来新型糖尿病治疗药物的研发提供一个全新方向和路径——这一历经四年的研究阐明了一个有助治疗糖尿病的分子靶点的作用机制,并发现了与之相关的一条全新调控糖代谢的信号通路。
该成果由我校生命科学学院吴乔教授课题组、林天伟教授课题组和化学化工学院黄培强教授课题组合作完成。日前,论文已在线发表在国际权威刊物《自然》姊妹期刊《自然-化学生物学》上。
2008年,吴乔教授课题组发现了一个与糖代谢调控密切相关的新靶点——名为Nur77的基因转录调控因子。但是,当时的实验结果却表明,这个分子对血糖的作用是提高而不是降低。
尽管这一研究成果发表在当年的《自然-化学生物学》杂志上,但吴乔及课题组并未满足于此。“究竟这样一个能够调控血糖水平的小小分子里蕴藏着怎样的‘玄机’?如果能找到一个药物来有效拮抗Nur77 的活性,岂不是就可以达到降血糖的目的?……”课题组决定将研究继续推进下去。
弄清楚Nur77的作用机理及其信号通路成为研究深入下去的最关键的“坎儿”,经过两三年的潜心研究,一个有“Nur77—LKB1—AMPK”三个分子参与其中的信号传导通路渐渐“浮出水面”。吴乔介绍说,AMPK为直接参与糖代谢调控的蛋白激酶,其活性可以通过一个名为LKB1的分子对其磷酸化得以“激活”,从而降低血糖。但不如愿的是,Nur77成为横亘在LKB1和AMPK之间的“障碍”——它将LKB1 “拽”在细胞核内,从而导致LKB1不能转运到细胞浆磷酸化AMPK,终使AMPK抑制血糖的能力大大下降。
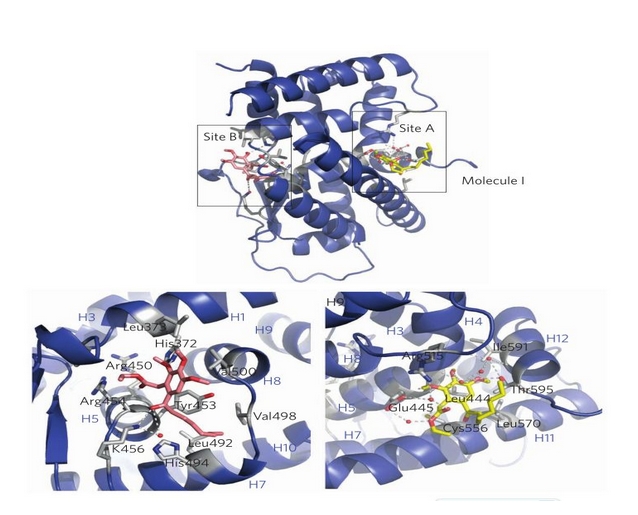
这样的发现为课题组带来的重要启示在于——如果能有效阻断Nur77和LKB1的结合,使得LKB1得以正常发挥对AMPK的激活作用,那么降低血糖便成为可能。通过与化学化工学院黄培强教授课题组合作,课题组很快发现了一个名为TMPA的化合物,它能够取代LKB1而与Nur77结合,从而“还”LKB1自由,使其从细胞核转运到胞浆激活AMPK活性,达到降血糖目的。更重要的是林天伟教授课题组获得了Nur77-TMPA共结晶体,从原子水平上进一步解释了TMPA结合Nur77的构象和精确位点,为今后设计和研发新型糖尿病药物提供了必不可少的结构基础。吴乔指出,从这个意义上说,TMPA也因此或可成为一种新型糖尿病治疗药物的“雏形”。
目前,这一研究已完成了由基因缺陷引起的II型糖尿病和高脂饲养诱导的非基因型II型糖尿病小鼠的体内实验,效果良好。吴乔说,下一步,课题组将进行相关临床前实验,并根据Nur77-TMPA共结晶结构进行化合物的改造,使其在未来成药时更加低毒高效。
新闻背后:只有学科交叉合作才能出高水平成果
采访中,除了成果本身外,吴乔教授提及次数最多的便是“学科交叉合作”一词。吴乔深有感触地说,若不是得益于与林天伟教授课题组和黄培强教授课题组的“精诚”合作,研究之路可能会更加曲折漫长。
在这个长达四年的研究中,三个课题组各负其责,各尽其职:以分子细胞生物学为研究方向的吴乔教授课题组负责“摸清”Nur77这一糖尿病治疗靶点的分子机制及其信号通路,并建立模型筛选降血糖化合物;林天伟教授课题组负责从结构生物学的角度来揭示TMPA与Nur77结合的构象和精确位点;黄培强教授课题组则负责“阻断” Nur77与LKB1结合的化合物合成。
事实上,早在2006年,吴乔教授课题组便与黄培强教授课题组建立了良好紧密的合作关系。从那时起迄今,黄培强教授课题组已为吴乔教授课题组合成了100多个化合物,建立了独特的具有特定靶标的化合物数据库。一旦需要,便能迅速根据模型从化合物库中筛选合成出“对路”的化合物。继而,林天伟教授课题组则集中“火力”解破共结晶的精密结构,共同开启了降血糖药物改造和临床前研究的征程。
吴乔说,也正是因为平日合作的“惯势”,才使得自己的课题组一遇到相关瓶颈时,便会自然而然地求助于“合作伙伴”。“目前,‘单打独斗’已很难再出高水平成果。通过与不同学科课题组甚至是与校外单位的合作,自己的视野开阔了,思路拓展了,研究之路也越走越宽。”
(宣传部 李 静)
编辑:郭露葳、钟蔚雯


