
近日,厦门大学神经科学研究所张云武教授团队在著名杂志Cell Death & Differentiation上发表题为RPS23RG1 modulates tau phosphorylation and axon outgrowth through regulating p35 proteasomal degradation的最新研究成果。该研究揭示了一条新的调控tau蛋白磷酸化的途径,为治疗tau蛋白病提供了新的策略。
Tau蛋白病(Tauopathies)是由过度磷酸化的tau蛋白聚集形成神经纤维缠结为特征的一类神经退行性疾病,包括阿尔茨海默病(Alzheimer’s disease, AD)、进行性核上性麻痹(Progressive superanuclear palsy, PSP)、额颞叶痴呆(Frontotemporal dementia, FTD)等。随着全球社会结构的老龄化,tau蛋白病患者比率迅速增加,给个人和社会带来巨大的经济及精神负担。尽管不同tau蛋白病的临床症状及体征大相径庭,但其共同特点为发病早期神经元和/或星形胶质细胞内出现异常磷酸化的tau蛋白。因此,深入阐明引起tau过度磷酸化的细胞及分子机制,对于治疗tau蛋白病显得尤为迫切和关键。
研究团队前期鉴定出一个新的Ib型蛋白RPS23RG1,发现该蛋白通过其跨膜区与腺苷酸环化酶(Adenylate Cyclase, AC)相互作用,进而调节AC/cyclic AMP/Protein Kinase A/Glycogen Synthase Kinase-3信号通路,抑制tau蛋白的过度磷酸化;并发现RPS23RG1可以调控PSD-93/PSD-95的泛素化及蛋白酶体降解过程,达到稳定神经突触结构与功能的作用,并证实此途径的异常参与AD的发生发展。相关成果先后发表在Neuron, Biological Psychiatry等杂志。
在此基础上,该团队最新发现RPS23RG1(RR1)的胞内羧基端区域能够与Cdk5激酶的激活蛋白p35的氨基端相互作用,介导p35的膜定位并影响其泛素化降解,从而调控在tau蛋白异常磷酸化过程中发挥重要作用的Cdk5激酶的活性(如图所示)。Rps23rg1基因敲除小鼠中p35蛋白及tau蛋白磷酸化水平升高,进而导致神经元轴突生长异常,而通过下调p35蛋白水平或抑制Cdk5活性都能改善Rps23rg1 KO小鼠神经元轴突异常及tau磷酸化水平。更重要的是,团队在tau蛋白病模型小鼠神经元中发现RPS23RG1蛋白水平显著下降而p35水平显著升高,并表现出神经元轴突生长异常,而通过恢复RPS23RG1蛋白水平可以降低tau蛋白病模型小鼠神经元中的p35水平及tau蛋白过度磷酸化,并逆转轴突生长缺陷。
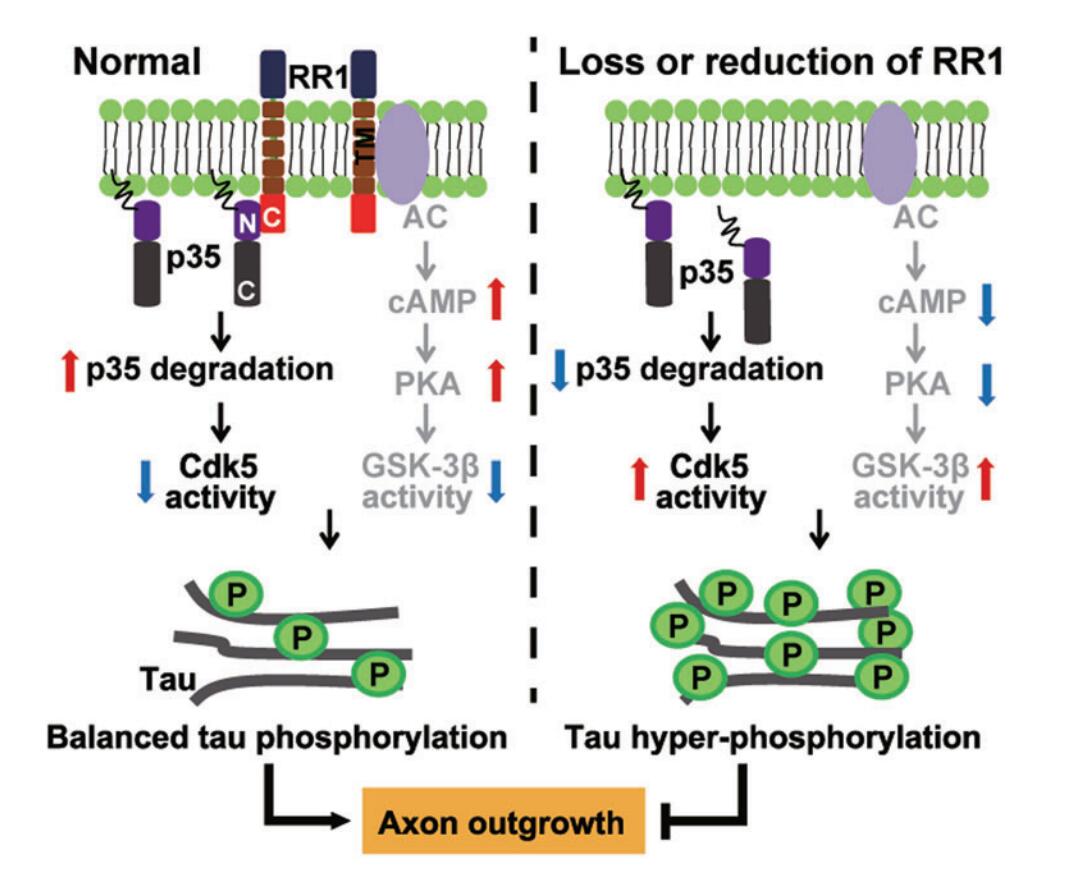
综上,该研究表明RPS23RG1通过其胞内羧基端与p35相互作用,介导p35膜结合和降解,从而抑制Cdk5活性,平衡tau磷酸化水平,促进轴突生长。此外,RPS23RG1的跨膜区与腺苷酸环化酶AC相互作用,抑制GSK3-β活性,同样控制tau过度磷酸化。提示RPS23RG1是改善tau过度磷酸化水平及治疗tau蛋白病的潜在靶点。

厦门大学医学院神经科学研究所博士后赵东栋为该研究第一作者,张云武教授为通讯作者。
原文链接:https://www.nature.com/articles/s41418-020-00620-y
(医学院张云武教授课题组)


