在肝癌、乳腺癌、胰腺癌等常见实体肿瘤的病程中,肿瘤组织常会出现纤维化加剧、硬度显著升高的变化。临床数据早已证实:肿瘤越“坚硬”,患者治疗后复发的风险越高、康复效果越差。但“硬肿瘤为啥更难治?”,这背后的关键机制长期以来都是医学界的未解之谜。
厦门大学生命科学学院团队联合陆军军医大学团队,揭示了免疫细胞为何一进入“硬板床”般坚硬的实体肿瘤,就会丧失战斗力、彻底“躺平”的核心机制,为癌症治疗开辟全新思路。这项重要成果也在《细胞》杂志上发表,引发广泛关注。
肿瘤变硬,“免疫特种兵”为何躺平
实体肿瘤可不是能让免疫细胞正常发挥作用的“软床”。厦大研究人员在肝癌患者的样本中发现,肿瘤组织高度变硬的区域,大量负责杀伤癌细胞的CD8+T免疫细胞(以下简称“T细胞”)已然“躺平”。
“T细胞‘躺平’,我们称之为‘T细胞耗竭状态’。”团队负责人陈兰芬解释道。在肿瘤高硬度微环境的持续刺激下,T细胞甚至进入了“终末耗竭状态”,这些原本战斗力极强的“免疫特种兵”,从“能打仗、敢打仗”慢慢变成“不想打、不能打”的状态,不仅“杀”不了癌细胞,对常规的免疫检查点治疗也反应不佳,“抗癌战斗力”彻底丧失且难以逆转。
这些“免疫特种兵”为何会放弃“战斗”?
研究团队找到了清晰的“捣乱路径”:肿瘤变硬后产生的机械压力,会像按动开关一样,激活T细胞表面的“机械力传感器”——Piezo1受体。被激活的“机械力传感器”随即“唤醒”大量“捣乱分子”——Osr2转录因子,而Osr2进一步招募“帮凶”HDAC3蛋白,抑制T细胞“杀敌武器”的合成。最终,“免疫特种兵”失去战斗力,变成“躺平兵”,再也无法对抗癌细胞。
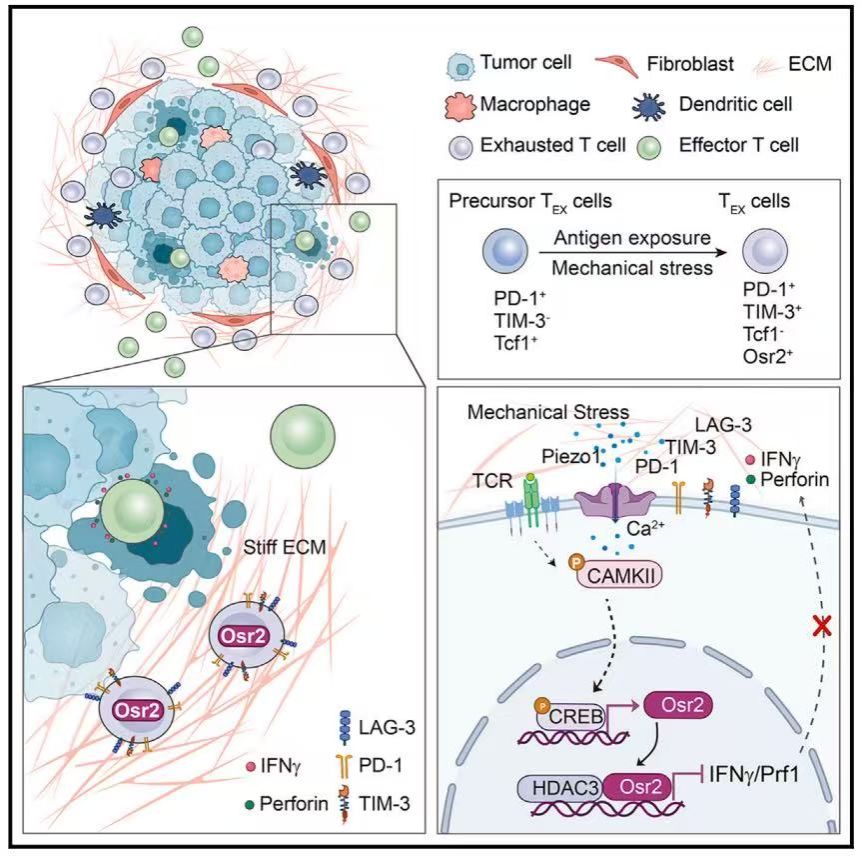
值得注意的是,“捣乱分子”Osr2很“挑剔”,它不影响早期T细胞的发育,而只有在肿瘤高硬度微环境和肿瘤抗原的持续刺激下,才会在T细胞中表达活化,发挥抑制作用,促进T细胞终末耗竭。“这是我们研究中最关键的发现,也为后续实体肿瘤疗法的研发提供了全新思路。”陈兰芬说。
挖口深井,啃下科研“硬骨头”
为了验证“肿瘤硬度导致T细胞躺平”的猜想,研究团队耗时半年攻坚,设计出一款体外细胞培养模型——硬度可调节的“细胞小床”。他们用不同软硬度的基质胶模拟肿瘤微环境,把T细胞分别安置在“硬板床”和“软床”上,直观追踪硬度对T细胞功能的影响。“这个模型的成功构建,为我们解开分子机制打下了最核心的基础。”团队成员侯永强介绍。
但研究中最难的,是验证Osr2转录因子的功能。一开始,团队尝试用转基因小鼠做实验,让小鼠体内细胞里的Osr2“持续过量工作”,想看看它对T细胞的影响。没想到,Osr2的抑制作用太过强大,如果没有严格控制Osr2的表达时间和表达量,会影响大量其他基因,最终“雪崩”一样导致小鼠细胞功能紊乱、无法获得正常的T细胞并研究其调控功能,实验被迫终止。
“碰壁后我们立刻换了思路。”陈兰芬说,团队改用特异性病毒感染技术:选取只能识别T细胞的病毒当“专属快递员”,把Osr2基因片段放进“快递盒”里,在T细胞特定阶段,精准送到细胞内部,从而特异性地研究其对T细胞功能的影响。如此一来,团队证实了,在肿瘤高硬度微环境下才出现的Osr2,会发挥“捣乱功力”,使得T细胞发展为终末耗竭状态,成为让T细胞彻底躺平的“罪魁祸首”。
从最初猜想到最终突破,团队花了至少5年的时间。“做研究就像挖井,挖一两米很容易,继续往下挖就难了,但如果挖100口浅井,不如集中精力挖一口深井。”陈兰芬回忆,研究过程中常遇到瓶颈,团队成员偶尔也会想放弃,但大家始终聚焦攻克“硬肿瘤难治”这个临床痛点,深耕自己的领域,大胆地向前走。

陈兰芬(左一)和团队成员
而能啃下这块“硬骨头”,跨学科的有组织科研功不可没。厦大团队联合陆军军医大学、清华大学、浙江大学等多个团队,集结了T细胞肿瘤免疫研究专家、生物力学建模能手、生物信息分析专家、分子检测技术人员等多领域人才,分工明确、优势互补,一步步攻克技术难关。
改造CAR-T疗法,癌症治疗未来可期
近年来,CAR-T细胞免疫疗法(以下简称“CAR-T疗法”)在白血病等血液肿瘤治疗中,疗效显著。但一旦遇到质地坚硬的实体肿瘤,就容易“失灵”,疗效大打折扣。
CAR-T疗法的核心是通过基因编辑改造患者自身的T细胞,让它能精准杀伤癌细胞。但面对实体肿瘤,改造后的T细胞很难进入内部,就算进去了,也会快速进入耗竭状态,变成“躺平兵”。
而厦大团队的这项研究,正好为解决这个问题提供了新思路。基于对“肿瘤硬度—T细胞耗竭”机制的理解,团队做了针对性改造:在原有CAR-T疗法的基础上,把T细胞中的Osr2基因“敲除”。结果发现,这样能有效缓解T细胞的耗竭,提高细胞存活率,显著抑制实体肿瘤的生长。
更重要的是,敲除Osr2不会影响T细胞早期发育及正常功能,也不会干扰人体的整体免疫稳态。目前,该项改造后的疗法已完成动物实验,正在向临床前实验推进。
“现有的CAR-T疗法不仅适用范围窄,价格也很昂贵。”陈兰芬表示,团队希望未来能进一步迭代这项技术,依托全国高校区域技术转移转化中心的研究平台推动技术落地,降低治疗成本,为肝癌、胰腺癌等难治性实体肿瘤患者带去新的治疗希望。
【团队名片】

厦门大学生命科学学院肿瘤免疫与器官大小调控创新团队,在周大旺教授与陈兰芬教授的带领下,依托厦门大学生物医学仪器共享平台、国家传染病诊断试剂与疫苗工程技术研究中心、分子诊断教育部工程研究中心等多个国家级与省部级科研平台,长期致力于Hippo信号通路在调控免疫稳态、器官尺寸、肿瘤发生及细胞命运决定中的核心机制研究,取得了一系列国际瞩目的原创性成果。团队在基础研究领域持续取得重大突破,多项研究成果发表于Cell、Nature Immunology、Cancer Cell等国际顶级学术期刊。其研究不仅具有理论创新性,更致力于解决临床难题。例如,团队揭示了实体瘤组织纤维化导致的力学微环境如何通过 Piezo1-Osr2 信号轴加剧CD8+ T细胞功能耗竭,为改善实体瘤中的免疫治疗效果提供了新靶点;同时,团队还发现了肝癌起始阶段存在异常的糖原积累现象,并创新性地提出糖原可通过“液-液相分离”的物理机制抑制Hippo通路活性,从而驱动肿瘤发生,这一发现对肝癌的早期诊断和干预具有重要意义。在成果转化方面,团队基于对Hippo通路关键激酶MST1/2的深入理解,已成功开发出首款靶向MST1/2的抑制剂,并积极推进其转化应用。未来,团队将进一步以临床需求为导向,加速前沿基础研究成果向创新药物和诊疗策略的转化,为促进我国生物医药产业的发展贡献力量。
(文/张夏 图片由受访者提供)
【往期文章】
1、飞机也能做“B超”,这项“无创体检”技术超精准:
https://news.xmu.edu.cn/info/1003/497092.htm
2、“微米级”较真,打造血糖监测“黑科技”:
https://news.xmu.edu.cn/info/1003/497712.htm
3、给船舶装上“智能管家” ——走进海嘉船舶综合信息系统:
https://news.xmu.edu.cn/info/1003/498912.htm
4、【科学的力量】医检界的“福尔摩斯” 一管揪出致病“真凶”
https://news.xmu.edu.cn/info/1003/499842.htm
5、【科学的力量】从城市废料到“绿色宝藏”:矿产资源回收技术的创新与突破
https://news.xmu.edu.cn/info/1003/500572.htm
6、【科学的力量】手机一拍榴莲“报数”,厦大马校团队AI打造“火眼金睛”!
https://news.xmu.edu.cn/info/1003/501352.htm
7、【科学的力量】轻小卫星,巡天瞰海的“太空慧眼”
https://news.xmu.edu.cn/info/1003/507062.htm
8、【科学的力量】“考古”“手艺”+AI医生 光影重生的传承
https://news.xmu.edu.cn/info/1003/508072.htm
9、【科学的力量】解锁氢燃料电池技术,为重卡装上“零碳心脏”
https://news.xmu.edu.cn/info/1003/509852.htm
10、【科学的力量】“微光”点亮视界——Mini-LED的技术革新之路
https://news.xmu.edu.cn/info/1003/512282.htm


